Alors que les scientifiques comprennent mieux les mystères de la physiologie humaine, il a été démontré à plusieurs reprises qu’une protéine appelée myostatine (MSTN) joue un rôle central dans la reproduction humaine. un nouveau Biologie de la reproduction et endocrinologie L’étude examine certains des rôles clés du MSTN dans la santé et les maladies reproductives féminines.

Étudier: Myostatine : un rôle multifonctionnel dans la reproduction et la fertilité féminines humaines : une brève revue. Crédit d’image : StudioMolekuul/Shutterstock.com
Introduction
Le MSTN, également connu sous le nom de facteur de différenciation de croissance 8 (GDF8), est codé sur le chromosome 2. Cette protéine réduit la croissance du muscle squelettique, empêchant ainsi une croissance excessive de ce tissu chez plusieurs espèces de mammifères et de poissons.
MSTN fait partie de la superfamille des facteurs de croissance transformants-β (TGF-β), qui comprend également les facteurs de différenciation de croissance (GDF), les protéines morphogénétiques osseuses (BMP), le TGF-β, les activines, les inhibines et l’hormone anti-mullérienne (AMH) . ) . La famille de protéines TGF-β régule la prolifération et la différenciation cellulaire, la cicatrisation, la fonction immunitaire et les pathologies squelettiques, en plus du cancer et de la fibrose.
AMH, BMP15 et GDF9 se trouvent à des niveaux élevés dans le système reproducteur féminin. Récemment, on a découvert que MSTN joue également un rôle important dans ce système.
Myostatine au début du développement
MSTN est exprimé dans le muscle squelettique de l’embryon en développement. Son niveau est le plus élevé en ce moment; cependant, on le trouve aussi à maturité.
D’autres sites MSTN comprennent le tissu adipeux et le cœur. L’absence de MSTN provoque une hyperplasie des cellules musculaires.
Le MSTN agit par l’intermédiaire du récepteur d’activine de type II ou IIb à la surface cellulaire, où il régule à la baisse la prolifération et la différenciation des cellules souches musculaires par plusieurs voies. Le résultat est une réduction des protéines des fibres musculaires à l’âge adulte et, par conséquent, une réduction de la masse musculaire.
D’autres activités du MSTN comprennent l’homéostasie de l’énergie cardiaque et la prévention de la prolifération des ventricules en réponse à l’ischémie et à l’insuffisance cardiaque. Dans le diabète de type 2, le MSTN est également régulé positivement, comme chez les personnes obèses ayant des niveaux d’insuline élevés. Avec l’exercice, la sensibilité à l’insuline augmente, indiquant un rôle pour le MSTN dans la régulation de l’absorption et de l’utilisation du glucose par les cellules musculaires.
Les niveaux de MSTN sont élevés chez les patients atteints de cancer, d’insuffisance cardiaque ou rénale et du syndrome d’immunodéficience acquise (SIDA), au cours duquel cette protéine régule probablement l’atrophie des cellules musculaires en cas de stress. Les personnes âgées et celles confinées au lit pendant de longues périodes ont également des niveaux plus élevés de MSTN.
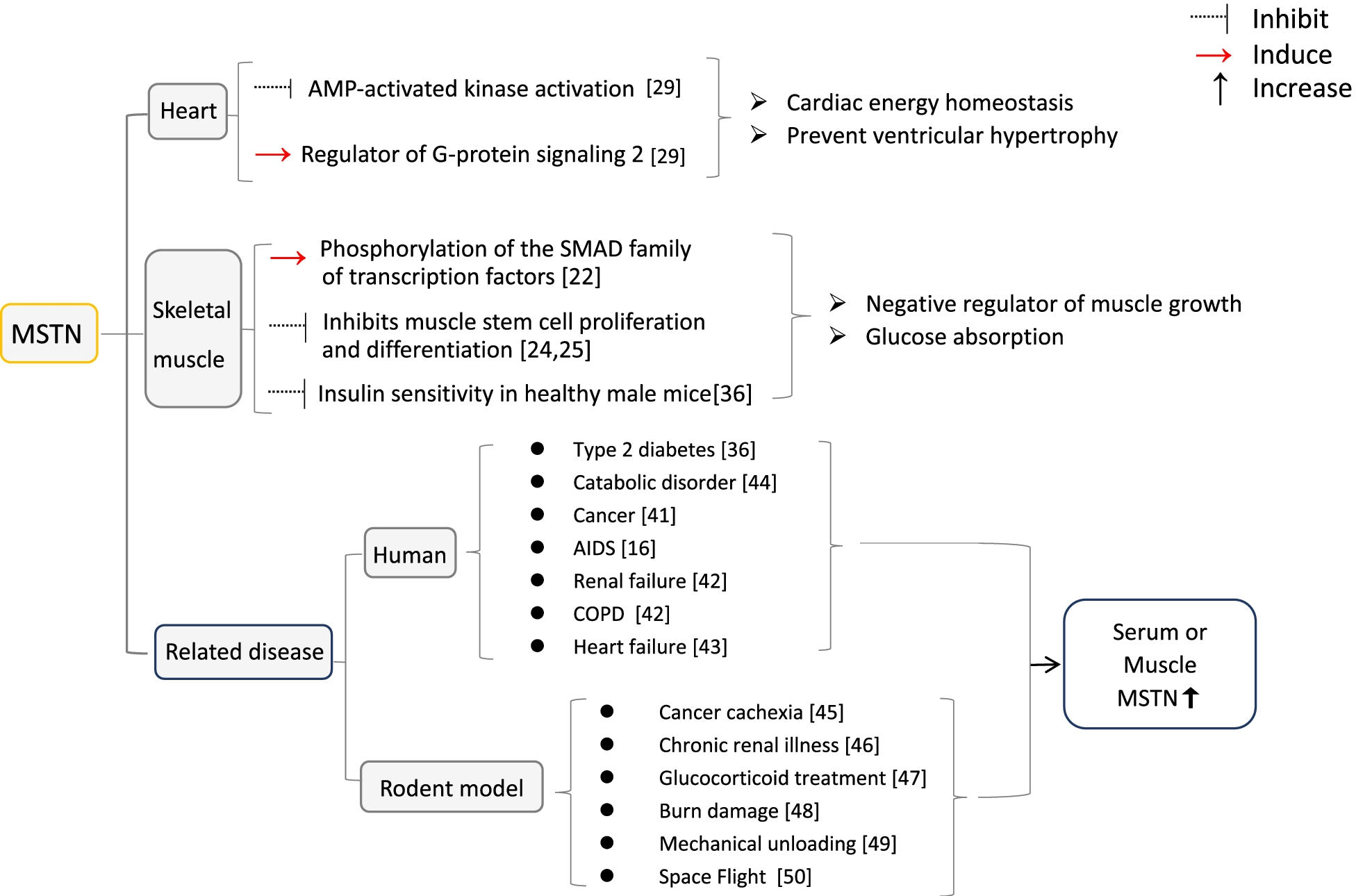
Résumé des fonctionnalités MSTN
Myostatine dans la reproduction féminine
MSTN régule la fonction ovarienne. De plus, cette protéine peut réguler la croissance des gonades, et son absence semble être associée à une diminution de la fertilité chez les animaux. L’enzyme limitant la vitesse de la voie de synthèse des stéroïdes, le régulateur aigu stéroïdogène (StAR), est également régulée à la baisse par le MSTN.
Le MSTN est présent dans les cellules de la granulosa ovarienne qui convertissent la testostérone en estradiol grâce à l’activité de l’enzyme aromatase, ainsi que dans le liquide folliculaire, où il réduit les niveaux de progestérone. Alors que la testostérone est synthétisée par les cellules théca ovariennes, l’estradiol est essentiel à la physiologie reproductive féminine.
MSTN augmente la synthèse d’estradiol par une expression accrue de l’aromatase du cytochrome P450. Cette protéine augmente les niveaux des récepteurs de l’hormone folliculo-stimulante (FSH), favorisant ainsi les effets de cette hormone.
Par conséquent, l’effet du MSTN est probablement un aspect essentiel des réponses des gonadotrophines et de la production d’hormones sexuelles.
MSTN agit également par la régulation à la hausse du facteur de croissance du tissu conjonctif (CTGF), qui déclenche des voies de signalisation pour réguler le recrutement des cellules de la thèque ovarienne, réguler la croissance folliculaire et aider à assurer un bon apport vasculaire au corps lutéal. Les deux facteurs inhibent la prolifération des cellules de la granulosa.
Une augmentation du CTGF conduit également à des niveaux plus élevés de lysyl oxydase (LOX), une enzyme vitale pour la formation de la matrice extracellulaire (ECM). Par conséquent, le CTGF est indispensable pour la fonction coordonnée de divers types de cellules via des hormones ainsi que des facteurs autocrines et paracrines dans le follicule ovarien, résultant en un ovocyte mature.
Le MSTN est également essentiel pour réguler la croissance des cellules du cumulus, qui forment le complexe contenant le follicule en cours de maturation. Ceci est régulé par une interaction hormonale entre l’ovocyte et ses cellules folliculaires.
MSTN inhibe la pentraxine 3 (PTX3), qui joue un rôle central dans la fertilité féminine. PTX3 régule le processus crucial de formation de l’ECM, assurant ainsi une bonne expansion du complexe cumulus-ovocyte, de l’ovulation et de la fécondation. MSTN peut également être un facteur de régulation produit par l’ovaire pour réguler les processus intra-ovariens.
MSTN et pathologie ovarienne
Le MSTN, en augmentant les taux d’aromatase et d’œstradiol dans les cellules de la granulosa, peut être impliqué dans l’effet indésirable courant et parfois grave du traitement de la fertilité connu sous le nom de syndrome d’hyperstimulation ovarienne (SHO).
Dans le SHO, la stimulation du développement folliculaire ovarien entraîne une hypertrophie des ovaires. Il en résulte une extravasation de liquide riche en protéines du sang dans l’espace extracellulaire en raison de l’hyperperméabilité de la paroi vasculaire. Cette perméabilité vasculaire accrue résulte de la concentration élevée de gonadotrophine chorionique humaine (hCG), qui active la paroi des vaisseaux sanguins.
Étant donné que les taux d’œstradiol pré-hCG sont plus élevés chez les femmes qui développent un SHO, le rôle du MSTN est clair et pourrait aider au développement de nouvelles thérapies pour cette condition à l’avenir. De même, ces découvertes peuvent également aider au traitement du syndrome des ovaires polykystiques (SOPK), qui touche jusqu’à une femme sur dix en âge de procréer et est responsable de jusqu’à 75 % de l’infertilité chez les femmes due à l’anovulation.
Dans le SOPK, plusieurs follicules se développent avec des niveaux élevés d’androgènes et une ovulation altérée. Le MSTN est également élevé dans les cellules de la granulosa et les grands follicules antraux dans les ovaires du SOPK, ce qui indique que le MSTN a échappé à la régulation.
Le MSTN dans le liquide folliculaire est riche en SOPK et réduit par la suite l’expression de StAR et supprime l’expression de la progestérone. Seuls les patients obèses atteints du SOPK ont montré des niveaux élevés de MSTN, qui peuvent être associés à l’effet inhibiteur du MSTN sur le métabolisme du glucose dans les cellules de la granulosa-lutéine.
MSTN et procréation assistée
Les niveaux de MSTN prédisent les taux de grossesse chez les patientes qui ont subi in vitro fécondation/injection intracytoplasmique de spermatozoïdes-transfert d’embryons (FIV/ICSI-TE). L’implantation d’embryons pourrait également être prédite par l’expression de MSTN, car cette molécule peut inhiber la croissance des cellules musculaires lisses utérines et de l’épithélium endométrial, régulant ainsi ce processus important.
Ces résultats démontrent que MSTN joue un rôle essentiel pour assurer une grossesse réussie, soulignant l’implication possible des niveaux de MSTN dans la réponse ovarienne pendant la COH. [controlled ovarian hyperstimulation] traiter.”
MSTN et placenta
MSTN peut influencer le développement placentaire par ses effets sur les cytokines, qui régulent la croissance, la différenciation et l’invasion des trophoblastes, qui sont toutes essentielles à la bonne placentation de l’embryon. Au début de la grossesse, MSTN agit pour augmenter le niveau de follistatine-like 3 (FSTL3), qui est une protéine qui se lie aux membres de la superfamille TGF pour supprimer leur activité, en particulier celle de MSTN. Fait intéressant, le FSTL est jusqu’à 20 fois plus élevé dans le placenta que dans tout autre organe.
Lorsque FSTL3 est élevé dans le placenta et le sang au cours du deuxième trimestre, le risque de développer une prééclampsie est plus élevé. Cela pourrait être une réponse à l’hypoxie des cellules trophoblastiques et peut aider à prédire la future prééclampsie et la restriction de croissance intra-utérine (IUGR). En revanche, un faible FSTL3 réduit l’invasion des trophoblastes.
MSTN est exprimé à des niveaux inférieurs dans le placenta mature qu’en début de grossesse. À cette fin, cette protéine régule l’homéostasie du glucose dans le placenta et pourrait aider à traiter un large éventail d’affections, de l’insuffisance placentaire au diabète sucré gestationnel (DG). MSTN normal avec de faibles niveaux de FSTL3 dans le sang maternel et le placenta peut indiquer un DG
MSTN et physiologie utérine
MSTN induit la prolifération du myomètre du muscle utérin ; cependant, sa concentration varie au cours du cycle menstruel. Avec les activines, MSTN régule l’activité gonadique.
MSTN est également sensible aux hormones stéroïdes, car ses niveaux diminuent avec l’exposition à l’estradiol mais pas après un traitement à la progestérone. Cependant, les niveaux de MSTN sont plus élevés après la ménopause.
Dans la tumeur utérine commune appelée fibrome (léiomyome), l’activine A, MSTN et FSTL3 sont exprimées à des niveaux plus élevés que dans le tissu utérin normal, sans preuve d’une transcription plus élevée. Par conséquent, la signalisation MSTN anormale est liée à la croissance des fibromes, car cette molécule inhibe la croissance du muscle utérin sain mais induit une fibrose des cellules de léiomyome.
Ces protéines sont également augmentées dans l’adénomyose, suggérant qu’elles ont un effet local dans cette affection.
conclusion
Le MSTN a plusieurs fonctions dans différents tissus du système reproducteur humain, notamment son implication dans la voie stéroïdogène, la réponse des cellules de la granulosa et de la thèque ovarienne aux hormones gonadotrophines, la prolifération cellulaire et l’expression de nombreuses molécules de signalisation intermédiaires.
Ces résultats suggèrent que le MSTN peut jouer un rôle essentiel en influençant les processus de différenciation finale dans les follicules émergents..”
La découverte de niveaux aberrants de MSTN dans les maladies utérines, placentaires et ovariennes indique son rôle régulateur clé dans la maturation des ovocytes. De plus, l’administration de MSTN est associée à de multiples effets indésirables, notamment une dérégulation métabolique et une perte de masse musculaire.
Beaucoup plus de travail est nécessaire pour comprendre comment fonctionne MSTN ; cependant, ces observations peuvent conduire au développement d’approches thérapeutiques meilleures et/ou nouvelles en matière de santé reproductive.
- Wang, S., Fang, L., Cong, L., et coll. (202). Myostatine : un rôle multifonctionnel dans la reproduction et la fertilité féminines humaines : une brève revue. Biologie de la reproduction et endocrinologie. doi : 10.1186/s12958-022-00969-4.

