La pandémie actuelle de maladie à coronavirus 2019 (COVID-19), causée par l’épidémie rapide de coronavirus-2 du syndrome respiratoire aigu sévère (SARS-CoV-2), a considérablement affecté le système de santé et l’économie mondiaux. Plusieurs études ont rapporté que les personnes âgées, ainsi que celles souffrant de certaines comorbidités telles que l’obésité et le diabète, courent un risque accru d’infection grave par le SRAS-CoV-2.
Étudier: L’infection par le SRAS-CoV-2 affecte la voie de signalisation insuline/IGF dans les poumons, le foie, le tissu adipeux et les cellules pancréatiques via IRF1. Crédit d’image : Eterysun / Shutterstock.com
Arrière plan
Bien que la plupart des patients atteints de COVID-19 présentent des symptômes légers à modérés, 10 à 15 % développent des symptômes graves de type pneumonie. Chez certaines personnes, le COVID-19 provoque des lésions tissulaires et déclenche des anomalies métaboliques, qui peuvent inclure une synthèse anormale des lipides, de l’insuline et des acides aminés. Le mécanisme moléculaire sous-jacent associé à ces anomalies métaboliques reste à déterminer.
Des études antérieures ont révélé que la voie de signalisation insuline/insulin-like growth factor 1 (IGF) joue un rôle important dans le métabolisme énergétique. D’autres voies moléculaires associées à l’absorption et à l’utilisation d’énergie comprennent la voie aval AKT/mTOR/MAPK et les interactions ligand/récepteur qui initient la signalisation cellulaire via IRS/PI3K.
Une résistance à l’insuline ou des réponses insuline/IGF anormales se produisent en raison d’une perturbation de la voie de signalisation insuline/IGF dans les organes et les tissus. En plus de la résistance à l’insuline, une voie de signalisation insuline/IGF altérée conduit également à l’hyperglycémie, au diabète, à l’hyperlipidémie et à l’obésité.
Une étude antérieure a montré que l’inactivation systémique des récepteurs de l’insuline chez la souris déclenchait un diabète précoce. De plus, certaines souris sont mortes en raison d’une acidocétose.
L’inhibition de la voie de signalisation insuline/IGF dans le tissu adipeux entraîne une perte de tissu adipeux. Cette condition provoque également un syndrome métabolique sévère, démontrant que la signalisation insuline/IGF est vitale pour la fonction des cellules bêta pancréatiques.
Des études antérieures ont également montré que la désactivation des récepteurs de l’insuline dans les cellules bêta provoquait une réduction de la production d’insuline, une condition également connue sous le nom de diabète sucré. L’association entre la résistance à l’insuline et le dysfonctionnement pulmonaire chez l’homme a également été documentée dans la littérature. À ce jour, très peu d’études ont déterminé l’impact de l’infection par le SRAS-CoV-2 sur la voie de signalisation insuline/IGF.
À propos de l’étude
Dans un récent Métabolisme étude, les scientifiques évaluent l’impact du SRAS-CoV-2 sur la voie de signalisation insuline/IGF. Dans cet article, les chercheurs ont obtenu des données transcriptomiques à haut débit liées aux cellules et tissus infectés par le SRAS-CoV-2 à partir de bases de données publiques.
Les chercheurs ont également obtenu des données d’autopsie sur les poumons de patients témoins avec et sans COVID-19. En outre, ils ont évalué l’impact de l’infection par le SRAS-CoV-2 sur les organoïdes hépatiques dérivés de cellules souches pluripotentes humaines (hPSC).
La présente étude a évalué l’impact de l’IRF1 sur la signalisation de l’insuline à l’aide de cellules HEK293T et Calu3. Pour évaluer le rôle des facteurs de risque de COVID-19 tels que le sexe, l’âge, l’obésité et le diabète dans la régulation mécaniste, les scientifiques ont analysé divers transcriptomes de cellules et de tissus métaboliques, respiratoires et endocriniens humains.
Résultats de l’étude
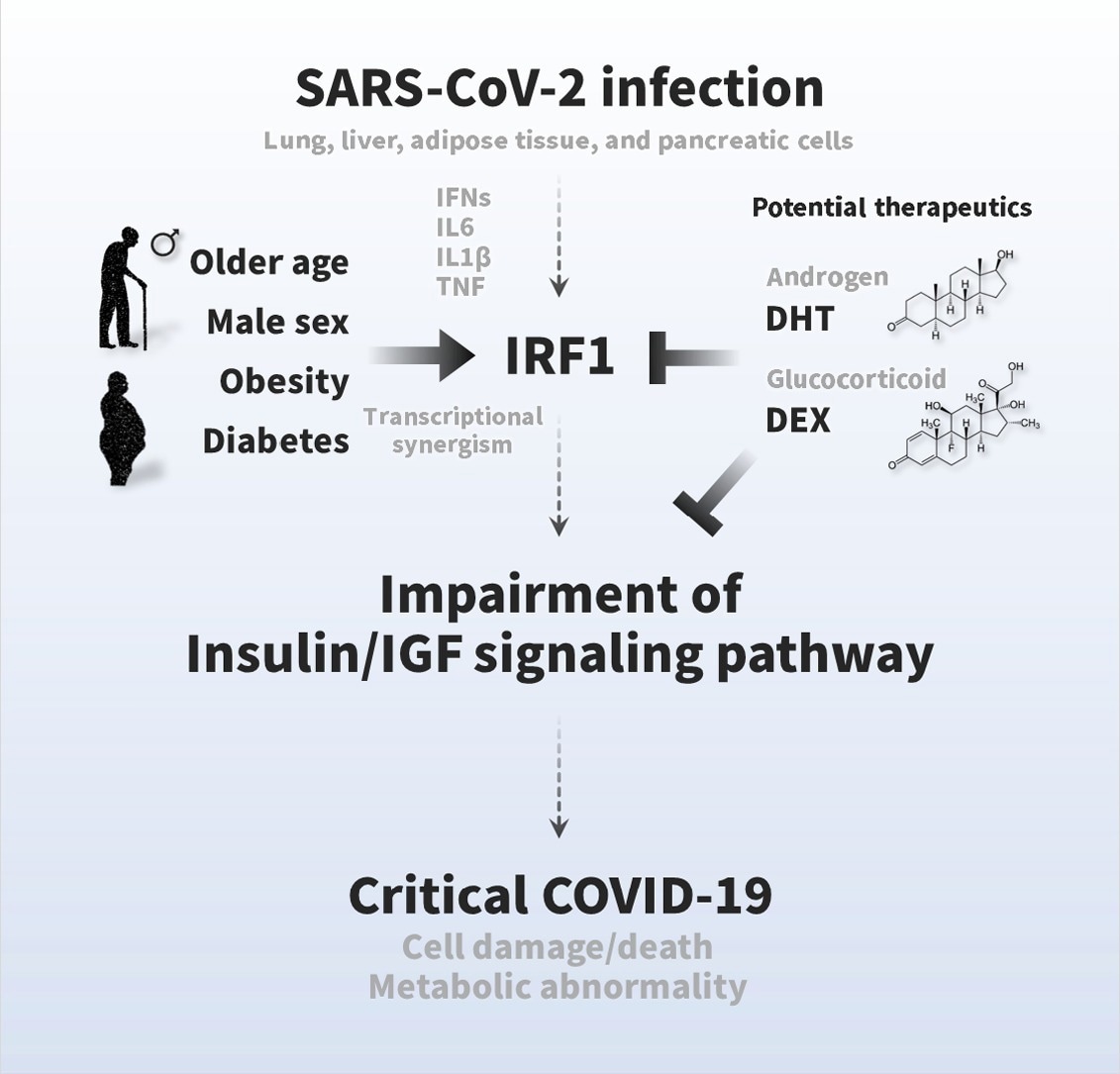
Une association forte a été observée entre une voie de signalisation altérée d’insuline/IGF et COVID-19 sévère. De plus, les chercheurs ont découvert que l’infection par le SRAS-CoV-2 affecte un large éventail de voies de signalisation insuline/IGF dans les poumons, le foie, les cellules pancréatiques et le tissu adipeux.
IRF1 s’est également avéré être associé à une voie de signalisation insuline/IGF altérée. Des études antérieures ont lié l’expression d’IRF1 au sexe masculin, à l’âge avancé, au diabète et au COVID-19. En fait, une expression plus élevée d’IRF1 a été associée à l’obésité, à l’âge avancé, au diabète et/ou à une variante génétique, qui pourrait être intensifiée en raison de la régulation positive d’IRF1 en réponse à l’infection par le SRAS-CoV-2.
Des études antérieures ont montré que le variant d’intron IRF1 rs17622656-A est abondamment présent dans les populations européennes et américaines. La présente étude rapporte que la pathologie du COVID-19 est régie par une expression plus élevée d’IRF1 et une expression plus faible des molécules de la voie de signalisation insuline/IGF.
Le traitement hormonal sous forme de dihydrotestostérone et de dexaméthasone a réduit efficacement l’expression du gène IRF1. Ces résultats ont conduit les chercheurs à émettre l’hypothèse que ce traitement pourrait augmenter la voie de signalisation insuline/IGF dans les cellules et les tissus infectés par le SRAS-CoV-2 et, par conséquent, améliorer la signalisation cellulaire.
Cette découverte indique clairement que l’infection par le SRAS-CoV-2 affecte non seulement les voies respiratoires, mais endommage également les cellules et les tissus endocriniens et métaboliques. Par conséquent, l’identification de la base moléculaire de ces observations pathologiques pourrait aider au développement de futures thérapies contre le COVID-19.
L’altération de la voie de signalisation insuline/IGF dans les cellules et les tissus du foie, des poumons et du pancréas entraîne le développement d’un dysfonctionnement multi-organique. Étant donné que le COVID-19 provoque une altération de la voie de signalisation insuline/IGF, il est également associé à la régulation à la baisse de plusieurs voies métaboliques, notamment le cycle du citrate, le métabolisme des lipides, la bêta-oxydation, le métabolisme des acides aminés et le métabolisme des glucides, et le transport respiratoire des électrons. .
Les chercheurs ont également souligné le potentiel de l’inflammation médiée par le COVID-19 pour induire une résistance à l’insuline dans divers cellules et tissus.
conclusion
L’étude actuelle a montré que les traitements à la dihydrotestostérone et à la dexaméthasone pourraient améliorer la résistance à l’insuline et les anomalies métaboliques chez les patients COVID-19. À l’avenir, davantage d’expériences physiologiques, pathologiques et pharmacologiques devraient être réalisées pour estimer l’efficacité clinique de ce traitement chez les patients COVID-19.
- Shin J, Toyoda S, Nishitani S, et autres. (2022) L’infection par le SRAS-CoV-2 affecte la voie de signalisation de l’insuline/IGF dans les poumons, le foie, le tissu adipeux et les cellules pancréatiques via l’IRF1. Métabolisme 133. doi:10.1016/j.metabol.2022.155236

