Au cours des deux dernières années, nous avons trouvé de nombreux rapports de symptômes persistants de la maladie à coronavirus (COVID-19), communément appelée « COVID à long terme ». Ces symptômes comprennent l’essoufflement, la fatigue, la myalgie, la perte de cheveux et la diminution des capacités cognitives.
Bien que les mécanismes et les facteurs contribuant à la longue durée du COVID restent insaisissables, les patients immunodéprimés ont tendance à souffrir partiellement d’une infection par le coronavirus 2 du syndrome respiratoire aigu sévère (SARS-CoV-2).
Il existe des preuves que les anticorps spécifiques contre l’immunoglobuline A (Ig) sont plus efficaces contre le SRAS-CoV-2 que les anticorps spécifiques contre les IgG et représentent une forme de neutralisation puissante précoce. Les anticorps IgA et IgG sont sécrétés dans le lait maternel des femmes allaitantes précédemment infectées par le SRAS-CoV-2 et chez celles qui ont été vaccinées contre le COVID-19.
 Étude : Élucidation de la détection persistante de l’ARN du SRAS-CoV-2 chez un patient présentant un déficit en NFκB en association avec l’ingestion de lait maternel : à propos d’un cas. Crédit d’image : Monthira/Shutterstock
Étude : Élucidation de la détection persistante de l’ARN du SRAS-CoV-2 chez un patient présentant un déficit en NFκB en association avec l’ingestion de lait maternel : à propos d’un cas. Crédit d’image : Monthira/Shutterstock
L’étude
Une nouvelle étude publiée dans la revue virus visait à rapporter les effets de la perfusion de plasma puis de l’ingestion de lait maternel en tant que traitement de l’infection persistante par le SRAS-CoV-2 chez un patient présentant un phénotype d’immunodéficience variable commune (DICV).
Le patient sélectionné présentait un polymorphisme du gène NFκB1, qui se caractérise par une immunosuppression et de graves déficiences dans la production de lymphocytes B et d’anticorps.
rapport de cas
Une femme de 32 ans s’est présentée avec des maux de gorge, de la toux, de la fièvre (38-38,5oC), ainsi que des maux de tête, de la fatigue, de l’anorexie et de la diarrhée, le 11 mars 2021, au cours des deux dernières semaines.
Une réaction en chaîne par polymérase quantitative en temps réel (RT-qPCR) de l’échantillon nasopharyngé a suscité l’ARN du SRAS-CoV-2.
Au suivi après un mois, le patient était asymptomatique. Cependant, les échantillons d’écouvillonnage nasopharyngé ont montré une charge virale de 1,99 × 107 copies d’ARN par ml. Le séquençage des gènes a révélé que la variante Gamma du SRAS-CoV-2 était l’organisme causal.
Une légère fièvre a persisté pendant 75 jours après la confirmation de l’infection, et le patient a également maintenu une perte de poids pendant quatre mois après l’infection. Pendant ce temps, ses niveaux de tomographie thoracique, d’électrocardiogramme (ECG) et de saturation en oxygène (SpO2) sont restés normaux. Les autres symptômes sont restés réfractaires pendant la phase post-COVID.
Environ trois mois après le diagnostic de COVID, 1,35 × 108 copies d’ARN/mL d’ARN du SRAS-CoV-2 ont été détectées par réaction en chaîne par polymérase en temps réel (RT-PCR) ; Le séquençage du génome entier a permis de confirmer le résultat.
Une analyse phylogénétique du maximum de vraisemblance (avec NextStrain) a établi la lignée Gamma. La probabilité de réinfection a été exclue.
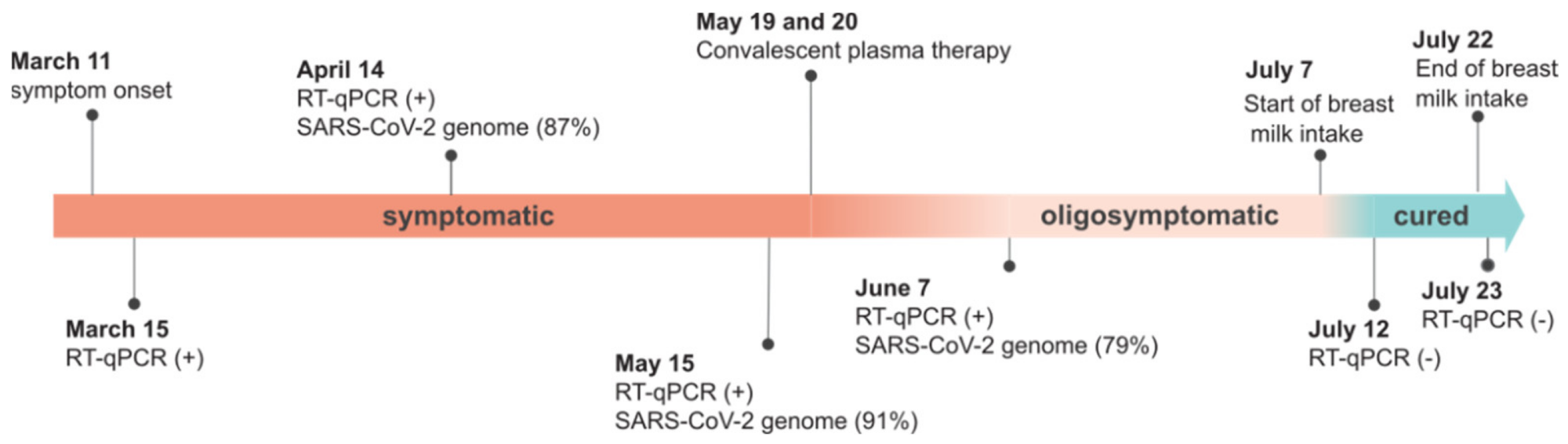 Chronologie du COVID-19 chez le patient présentant un déficit en NFκB. (+), positif ; (-), négatif. (%) représente le pourcentage de couverture du génome SARS-CoV-2 séquencé.
Chronologie du COVID-19 chez le patient présentant un déficit en NFκB. (+), positif ; (-), négatif. (%) représente le pourcentage de couverture du génome SARS-CoV-2 séquencé.
Le patient a été isolé et soigné à domicile sous surveillance médicale. Bien que cette évolution clinique du COVID-19 ait été considérée comme dérégulée, l’hyperinflammation était absente pendant 124 jours après le diagnostic.
Le 19 mai 2021, le patient a reçu 600 ml de plasma convalescent avec des titres d’IgG : 1:640, par voie intraveineuse de deux patients COVID-19, pendant deux jours consécutifs. Trois jours après la perfusion, sa maladie fébrile a disparu et la patiente a déclaré se sentir mieux. À ce moment, l’ARN du SRAS-CoV-2 persistait dans les échantillons d’écouvillon oropharyngés, comme l’a révélé un test RT-qPCR effectué le 7 juin 2021.
De plus, la patiente n’avait pas complètement récupéré, son appétit n’était pas revenu et elle se sentait toujours faible. L’infection asymptomatique est restée, posant un risque de transmission et même de progression vers un COVID-19 sévère.
Désormais, l’ingestion d’IgA spécifiques du SRAS-CoV-2, dérivées du lait maternel des femmes ayant reçu le vaccin COVID-19, a été suggérée. Cette stratégie était basée sur la découverte que les dimères IgA sont plus puissants que les monomères IgG pour neutraliser le SRAS-CoV-2.
Le lait maternel pasteurisé d’une mère vaccinée avec BNT162b2 (Pfizer-BioNTech) a été utilisé à cet effet : 180 ml par jour pendant deux semaines. L’alimentation était pratiquée de manière à ce que la patiente tienne le lait dans sa bouche pendant au moins trois minutes avant de l’avaler.
Juste une semaine après la perfusion de plasma convalescent, le nombre absolu de neutrophiles, de lymphocytes et de monocytes a doublé, suggérant une récupération hématopoïétique. Cependant, les lymphocytes ont diminué de moitié après une semaine, après l’ingestion de lait maternel, et ont montré une valeur autour de la limite supérieure de la plage normale.
Les altérations des paramètres mentionnés décrivaient l’état clinique de l’infection par le SRAS-CoV-2, qui a précédé l’impact des interventions thérapeutiques.
Il convient de noter qu’avant la perfusion de plasma convalescent, le nombre de cellules CD3+ et CD4+ a diminué de plus de la moitié des nombres habituels, qui ont été restaurés après la perfusion de plasma et l’ingestion de lait maternel. Cependant, aucun changement du rapport CD4+/CD8+ ou du nombre absolu de CD19+ n’a été observé pendant l’infection. Alors qu’après l’intervention, des réductions significatives des niveaux de ferritine sérique et de protéine C-réactive (qui avaient auparavant augmenté), laissaient entrevoir une forte activité neutralisante, suggérant un effet protecteur.
Le patient a complètement récupéré le 21 juillet 2021 ; cela a été confirmé par des résultats de test négatifs (RT-qPCR) d’échantillons d’écouvillons oropharyngés, 16 jours après le traitement. Le 24 novembre 2021, le patient est resté négatif pour COVID-19, sur la base des tests IgM et RT-qPCR sans réactif.
Ce rapport de cas marque une utilisation non conventionnelle d’anticorps sécrétoires spécifiques au lait maternel comme thérapie contre le COVID-19. On a émis l’hypothèse que les anticorps IgA sécrétés dans le lait maternel des femmes vaccinées contre le COVID-19 pourraient neutraliser le SRAS-CoV-2 soutenu dans divers organes de personnes récemment infectées, tels que les amygdales, l’oropharynx et le tractus gastro-intestinal.
Par conséquent, une telle intervention thérapeutique peut aider à éliminer l’infection chez les personnes immunodéprimées atteintes de COVID prolongé. Dans le cas présent, aucune nouvelle mutation dans le génome variant Gamma ou des polymorphismes mononucléotidiques (SNP) n’ont été observés pendant toute la période d’étude malgré le fait que le patient était immunodéprimé.
- Sabino, J., Amorim, M., de Souza, W., et al. (2022). Élucidation de la détection persistante de l’ARN du SRAS-CoV-2 chez un patient présentant un déficit en NFκB en association avec l’ingestion de lait maternel humain : à propos d’un cas. virus doi : 10.3390/v14051042.

